📄 Fusion of Multimodal Estimations by Extended State Hidden Markov Model: Application to Fetal Heart Rate Monitoring
#生物声学 #信号处理 #多任务学习 #医疗
✅ 7.0/10 | 前50% | #生物声学 | #信号处理 | #多任务学习 #医疗
学术质量 5.5/7 | 选题价值 1.5/2 | 复现加成 0.0 | 置信度 高
👥 作者与机构
- 第一作者:Baptiste Rault(Université Grenoble Alpes, CNRS, UMR 5525, VetAgro Sup, Grenoble INP, TIMC)
- 通讯作者:Bertrand Rivet(未明确说明,但提供了邮箱;机构为Université Grenoble Alpes, CNRS, Grenoble INP, GIPSA-lab)
- 作者列表:Baptiste Rault(Université Grenoble Alpes, CNRS, UMR 5525, VetAgro Sup, Grenoble INP, TIMC)、Julie Fontecave-Jallon(Université Grenoble Alpes, CNRS, UMR 5525, VetAgro Sup, Grenoble INP, TIMC)、Bertrand Rivet(Université Grenoble Alpes, CNRS, Grenoble INP, GIPSA-lab)
💡 毒舌点评
亮点:扩展HMM状态变量以显式建模“观测是目标信号、混淆信号还是噪声”的思路巧妙且可解释,有效提升了融合算法在真实临床数据上的抗混淆能力(FuSEmHR的RMC中位数降至1.5%)。短板:算法复杂度急剧增加(融合1分钟数据从35ms升至8秒),且最终版本严重依赖可靠的参考信号(mHR),限制了其在未知或不稳定干扰下的应用;更遗憾的是,论文未开源任何代码或数据,让“可复现性”成了一纸空文。
🔗 开源详情
- 代码:论文中未提及代码链接。
- 模型权重:未提及。
- 数据集:论文描述了一个来自格勒诺布尔大学医院的临床数据集,但未提供公开获取方式。
- Demo:未提供在线演示。
- 复现材料:论文描述了数据采集设置和性能指标,但未提供模型训练细节、超参数配置、预训练检查点或详细的附录说明。
- 论文中引用的开源项目:论文引用了前序工作[12, 16, 17],但未明确说明依赖的开源工具或模型。
- 总结:论文中未提及任何开源计划。
📌 核心摘要
- 要解决什么问题:非侵入式胎儿心率(fHR)监测中,单一模态(如腹部ECG或PCG)存在信号质量差、易与母体心率(mHR)混淆的问题。现有基于隐马尔可夫模型(HMM)的融合方法未能显式处理观测信号可能是目标信号、混淆信号或噪声这三种情况。
- 方法核心是什么:提出一种扩展状态HMM(FuSE)用于融合ECG和PCG模态的fHR估计。核心是在原有隐藏状态(fHR)基础上,为每个模态增加一个离散变量Z,用于指示当前观测是真实fHR(H)、被mHR混淆(C)还是噪声(N)。进一步地,若mHR参考信号可用,可在模型中显式利用它来优化“混淆”情���下的发射概率,形成FuSEmHR变体。
- 与已有方法相比新在哪里:相比传统的HMM融合方法(仅考虑“信号+噪声”或“纯噪声”两种情况),新方法引入了第三种关键状态“并发信号(混淆)”,并允许利用先验的干扰信号(mHR)信息来细化模型,从而更精确地区分和利用来自不同模态的观测。
- 主要实验结果如何:在包含38名受试者、约20小时临床数据的集上测试。与基线HMM融合方法(Fus[12])相比,FuSEmHR在准确度(RGA,与CTG参考的一致性)上中位数从79%提升至88%;在抗母体混淆率(RMC)上中位数从3%降至1.5%。其表现在大多数受试者上优于单模态ECG或PCG。关键实验数据如下表所示:
| 方法 | RGA中位数 (%) | RMC中位数 (%) | 备注 |
|---|---|---|---|
| ECG | 46 | 15.5 | 单模态 |
| PCG | 68.5 | 5 | 单模态 |
| Fus [12] | 79 | 3 | 基线融合方法 |
| FuSE | 82.5 | 3 | 本文方法(未用mHR信息) |
| FuSEmHR | 88 | 1.5 | 本文最终方法(用mHR信息) |
注:数据来源于论文图2和图4的描述。
- 实际意义是什么:该方法为结合ECG和PCG进行更鲁棒、准确的无创胎儿心率监测提供了一种有效框架,有望减少临床误判(如误将mHR当作fHR),从而降低不必要的医疗干预。
- 主要局限性是什么:计算复杂度显著增加,不利于实时性要求极高的应用;FuSEmHR变体的性能依赖于可靠获取母体心率参考信号;模型参数需要从数据中学习,其泛化性有待更多样化数据验证。
🏗️ 模型架构
论文提出的模型是对传统双模态HMM(图1)的扩展。其整体架构旨在融合来自ECG和PCG两个模态的fHR估计序列,最终输出一个更准确、更少混淆的fHR序列。
输入:两个模态的观测序列:M⁽¹⁾ₖ (来自ECG的fHR估计) 和 M⁽²⁾ₖ (来自PCG的fHR估计),其中k为时间索引。 输出:隐藏状态序列的估计 ŜH₀:ₜ,即融合后的fHR。
核心组件与数据流:
- 扩展状态变量 Xₖ:这是模型的核心创新。在任意时刻k,状态不再仅仅是离散的胎儿心率值 ŜHₖ,而是扩展为一个三元组 Xₖ = (ŜHₖ, Z⁽¹⁾ₖ, Z⁽²⁾ₖ)。
- ŜHₖ:表示真实的胎儿心率值(隐藏信号SH)。
- Z⁽ⁱ⁾ₖ (i=1,2):是一个离散变量,其取值∈{H, C, N}。它表示对模态i在时刻k的观测 M⁽ⁱ⁾ₖ 的分类:
- Z⁽ⁱ⁾ₖ = H:观测 M⁽ⁱ⁾ₖ 是胎儿心率信号(SHₖ)加噪声。
- Z⁽ⁱ⁾ₖ = C:观测 M⁽ⁱ⁾ₖ 是并发/混淆信号(在应用中即为母体心率SCₖ,此处为mHR)加噪声。
- Z⁽ⁱ⁾ₖ = N:观测 M⁽ⁱ⁾ₖ 仅为噪声。
- 转移概率:扩展状态Xₖ的转移概率被分解为:
- P(ŜHₖ | ŜHₖ₋₁):胎儿心率状态本身的转移概率,与传统HMM相同。
- P(Z⁽ⁱ⁾ₖ | Z⁽ⁱ⁾ₖ₋₁):每个模态的“观测类型”变量Z⁽ⁱ⁾自身具有马尔可夫性,其转移概率描述了观测类型(如“正常”、“混淆”、“噪声”)如何随时间变化。
- 发射概率:对于每个模态i,观测 M⁽ⁱ⁾ₖ 的发射概率不再简单地依赖于 ŜHₖ,而是同时依赖于 ŜHₖ 和 Z⁽ⁱ⁾ₖ。具体形式见公式(9)。根据Z⁽ⁱ⁾ₖ的取值,使用不同的概率分布(L⁽ⁱ⁾H, L⁽ⁱ⁾C, L⁽ⁱ⁾N)来描述观测。
- FuSEmHR的特别设计:当获得可靠的并发信号(mHR)参考 Wᶜₖ 时,在 Z⁽ⁱ⁾ₖ = C 的情况下,发射概率 P(M⁽ⁱ⁾ₖ | Wᶜₖ, Z⁽ⁱ⁾ₖ = C) 会利用 Wᶜₖ 信息来更精确地建模观测,如公式(11)所示。这提供了更强大的先验信息来区分fHR和mHR。
- 推理:使用扩展后的Viterbi算法(公式更新为基于状态Xₖ)来寻找最可能的隐藏状态序列 ŜH₀:ₜ。对于在线应用,可以省略回溯步骤,直接取每个时刻的最优状态。
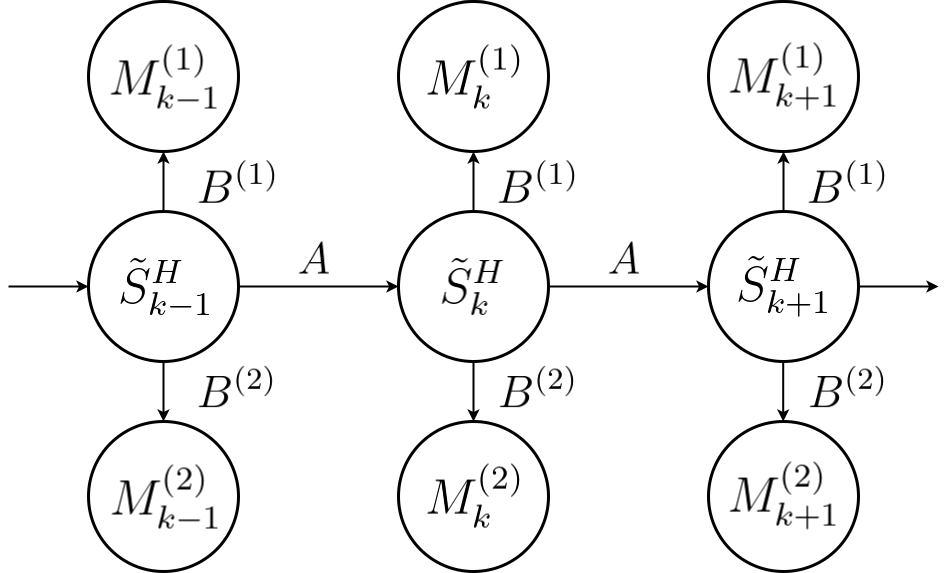 图1展示了传统的双模态HMM图模型。论文提出的FuSE/FuSEmHR模型在此基础上,将每个观测变量M⁽ⁱ⁾ₖ与一个隐含的“类型变量”Z⁽ⁱ⁾ₖ(表示观测是H, C, N)相连,并允许Z⁽ⁱ⁾ₖ序列具有自身的转移概率。
图1展示了传统的双模态HMM图模型。论文提出的FuSE/FuSEmHR模型在此基础上,将每个观测变量M⁽ⁱ⁾ₖ与一个隐含的“类型变量”Z⁽ⁱ⁾ₖ(表示观测是H, C, N)相连,并允许Z⁽ⁱ⁾ₖ序列具有自身的转移概率。
💡 核心创新点
- 显式建模观测的三种类型:传统融合模型仅考虑“目标信号+噪声”或“纯噪声”。本文创新性地引入第三个状态“并发信号+噪声”(Z⁽ⁱ⁾ₖ = C),直接针对胎儿心率监测中mHR混淆这一核心临床难题,使模型更具解释性和针对性。
- 利用并发信号的先验信息:提出的FuSEmHR变体,允许在推理过程中直接输入可靠的并发信号(mHR)参考。这将外部知识融入概率模型,在Z⁽ⁱ⁾ₖ = C的情况下显著优化了发射概率的计算,是提升性能的关键。
- 对基础HMM融合框架的系统改进:论文清晰地展示了如何从Souriau等人[12]的基础HMM融合框架出发,逐步扩展(引入Z变量 -> 利用先验信号),并通过实验验证每一步改进的有效性(Fus -> FuSE -> FuSEmHR),方法演进逻辑严谨。
🔬 细节详述
- 训练数据:数据集来源于格勒诺布尔大学医院,包含38名孕晚期(37-40周)孕妇的录音,平均时长约30分钟,总计约20小时。包括胸腔ECG(提供mHR参考)、腹部ECG、腹部PCG和腹部CTG(提供fHR参考)。
- 损失函数:未提及显式的损失函数。模型参数(转移矩阵A、发射概率L⁽ⁱ⁾的先验P(Z⁽ⁱ⁾)及具体分布参数)是从真实数据集中学习得到的(具体学习方法未详细说明)。
- 训练策略:未说明具体的学习算法、迭代过程或优化目标。仅提到参数“从真实数据集中确定”。
- 关键超参数:HMM的状态空间大小取决于fHR的离散化粒度(未说明),以及Z变量的三个状态(H, C, N)。计算复杂度与状态空间大小直接相关,FuSEmHR处理1分钟数据需8秒。
- 训练硬件:未说明。
- 推理细节:采用Viterbi算法进行序列解码。对于在线场景,使用不带回溯的逐帧最大后验估计。FuSEmHR需要实时获取mHR参考信号。
- 正则化或稳定训练技巧:未说明。
📊 实验结果
主要实验结果已在核心摘要的表格中列出。以下结合图表补充关键结论:
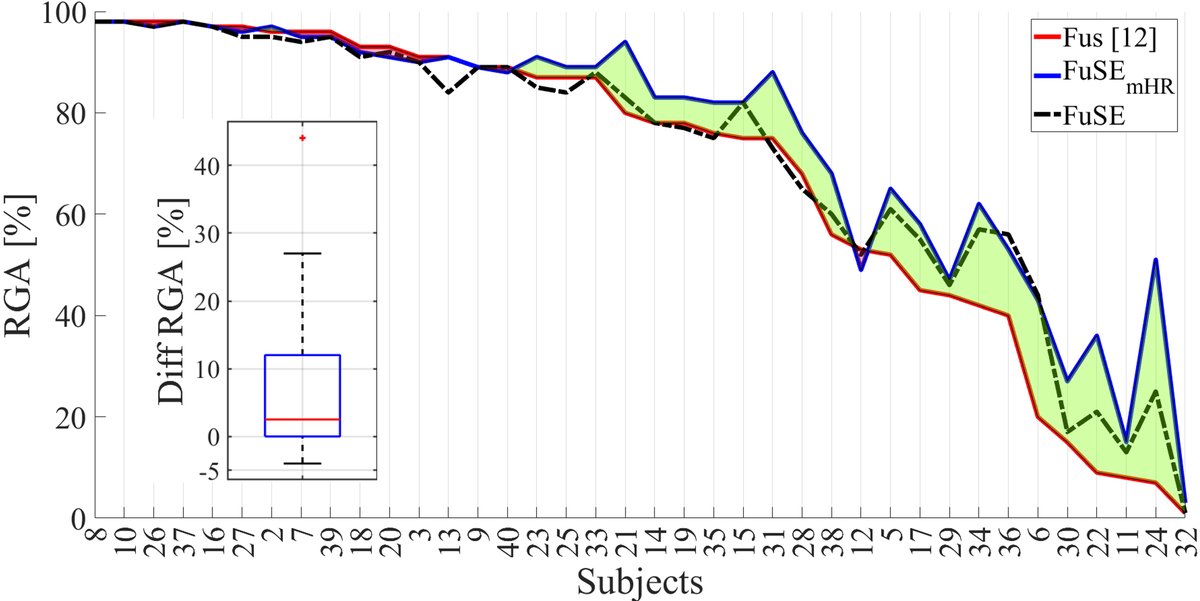 图2(RGA箱线图)显示:ECG和PCG单模态性能差异大且不稳定。三种融合方法(Fus, FuSE, FuSEmHR)的RGA中位数和稳定性(箱体范围)均优于单模态,且FuSEmHR最佳。
图2(RGA箱线图)显示:ECG和PCG单模态性能差异大且不稳定。三种融合方法(Fus, FuSE, FuSEmHR)的RGA中位数和稳定性(箱体范围)均优于单模态,且FuSEmHR最佳。
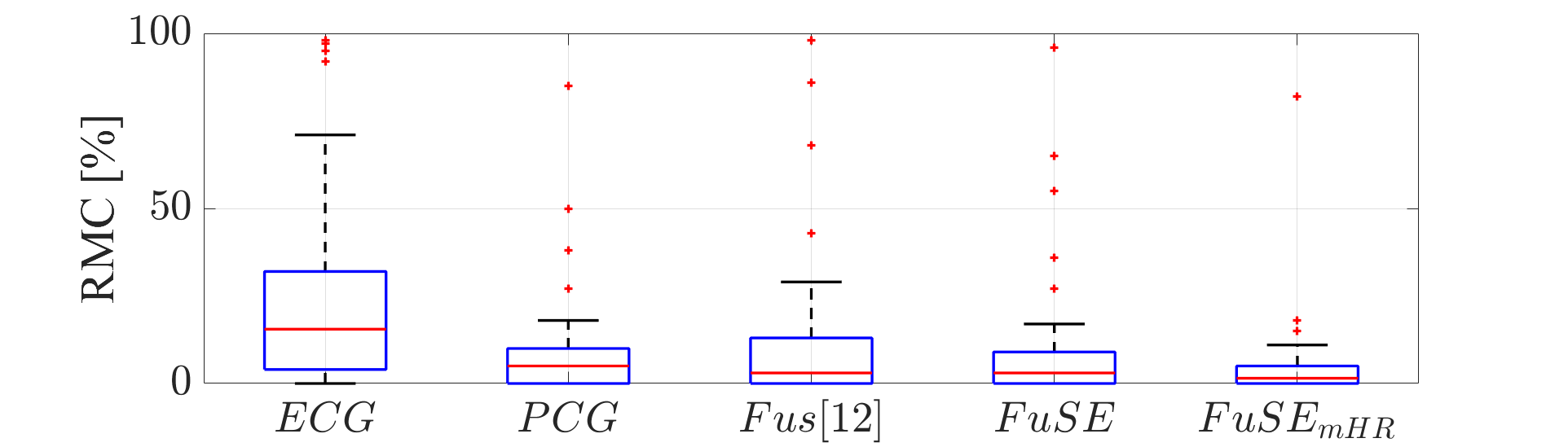 图3(逐个受试者的RGA对比)显示:对于原始Fus方法表现较差的后半段受试者,FuSEmHR(红线)相比Fus(蓝线)有显著提升(绿色区域),表明其鲁棒性增强。左侧箱线图量化了这种提升幅度(多数为正向提升)。
图3(逐个受试者的RGA对比)显示:对于原始Fus方法表现较差的后半段受试者,FuSEmHR(红线)相比Fus(蓝线)有显著提升(绿色区域),表明其鲁棒性增强。左侧箱线图量化了这种提升幅度(多数为正向提升)。
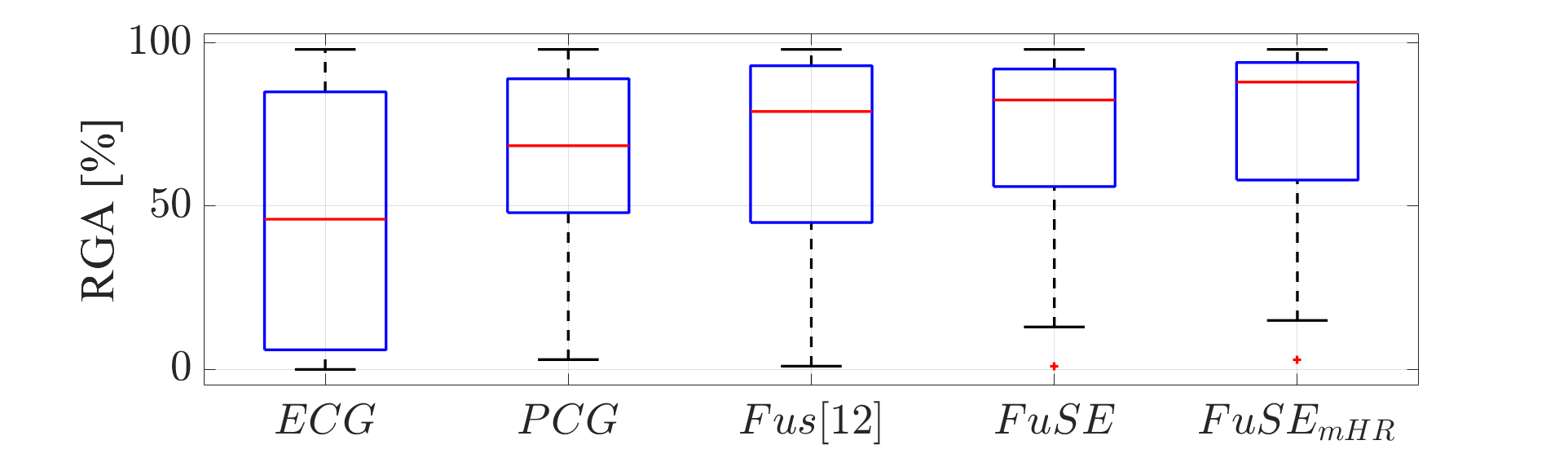 图4(RMC箱线图)显示:ECG的母体混淆率最高。FuSEmHR的RMC中位数和上四分位数均为最低,证实了其利用mHR信息后抗混淆能力的显著优势。
图4(RMC箱线图)显示:ECG的母体混淆率最高。FuSEmHR的RMC中位数和上四分位数均为最低,证实了其利用mHR信息后抗混淆能力的显著优势。
与最强基线的差距:FuSEmHR在RGA(中位数88% vs 79%)和RMC(中位数1.5% vs 3%)两个关键指标上均优于最强基线Fus [12]。 关键消融实验:论文通过Fus -> FuSE -> FuSEmHR的递进对比,实质上进行了消融分析,证明了引入Z变量(FuSE)和进一步引入mHR先验(FuSEmHR)各自带来的性能增益。 计算成本:FuSEmHR的计算时间(8秒/分钟数据)远高于Fus [12](35毫秒/分钟数据),是其主要代价。
⚖️ 评分理由
- 学术质量:5.5/7 - 方法设计有明确的临床问题驱动,逻辑清晰,扩展合理。在真实数据集上进行了充分实验,指标选择恰当,结果具有说服力。但创新属于框架内的改进,未提出新的模型理论,且部分技术细节(如参数学习)未公开。
- 选题价值:1.5/2 - 解决的是胎儿监护中的实际痛点,应用价值明确。但领域垂直,与更广泛的音频处理研究交叉有限。
- 开源与复现加成:0.0/1 - 论文未提供代码、数据或关键复现参数,严重阻碍了社区的复现和应用。